临床研究院/疑难疾病精准研究中心-施雷雷团队开发分子靶向生物活性光敏剂用于乏氧恶性肿瘤的光动力免疫治疗
光动力疗法(PDT)是利用光敏分子在特定波长光激发下产生“光动力”反应起到抗肿瘤作用的一种疗法。PDT过程中,光敏药物能够通过能量或者电子转移生成活性氧簇(ROS)。ROS能与附近的生物大分子发生反应,产生细胞毒性进而杀伤肿瘤细胞。与传统疗法相比,PDT的优势在于能够利用光的高时空分辨性进行精确有效的治疗,因此副作用较小。然而由于肿瘤细胞内的还原性谷胱甘肽浓度较高,能够迅速淬灭光敏分子在光照下产生的活性氧自由基;另外绝大部分的光敏分子产生活性氧自由基依赖分子氧(O2)的浓度,而实体瘤内部的乏氧微环境会很大程度限制光动力治疗的效果。
为了解决上述光动力治疗过程中的问题,临床研究院/疑难疾病精准研究中心施雷雷研究员带领课题组在前期工作中提出了分子靶向光动力治疗的策略(Adv. Mater. 2022, 34, e2206659),通过在光敏分子上引入组蛋白去乙酰化酶(HDACs)的药效团,使该分子在发挥光动力治疗作用的同时抑制HDACs活性以提高肿瘤细胞的乙酰化水平,诱导肿瘤细胞凋亡,缓解肿瘤组织的乏氧状态,从而增强光动力的治疗效果。
在前期工作基础上,研究团队进一步对生物活性光敏剂分子结构进行了优化,发展了一种不依赖于肿瘤组织氧气浓度的I型生物活性光敏剂分子QTANHOH,能够实现小鼠原位乳腺癌的光动力免疫治疗。体外实验表明,乏氧状态下QTANHOH在光激发下也能够高效地产生ROS,并对肿瘤细胞有很强的杀伤效果。同时,体内和体外实验证明该生物活性光敏剂能够激活肿瘤组织的免疫微环境从而增强光动力治疗效果。该多功能的光敏分子QTANHOH为分子靶向光免疫治疗的光敏剂的开发提供了重要策略。
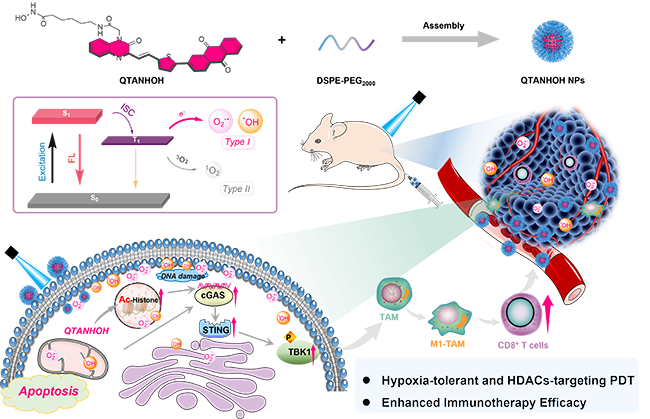
图1 光敏剂QTANHOH进行分子靶向光动力免疫治疗示意图
研究团队检测不同的指示剂发现光敏剂分子在光照下能够产生I型活性氧自由基。ESR实验也检测到了超氧自由基的存在。
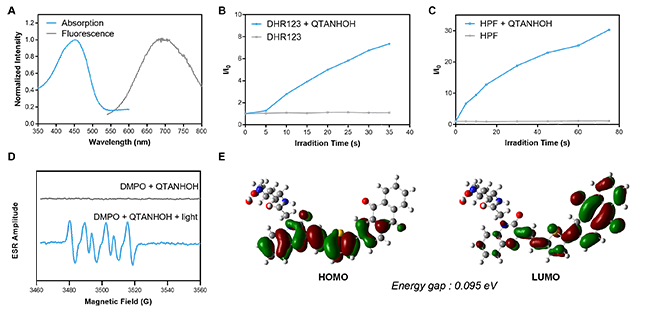
图2 光敏剂的光学性质表征
在乏氧条件下,细胞层面也能够检测到I型活性氧的存在。光照下,QTANHOH对三种乳腺癌细胞系(4T1、MDA-MB-231、MCF 7)有很强的杀伤效果。此外,由于光敏剂能够抑制HDAC的活性,即使在不光照的条件下,对癌细胞也有明显的杀伤能力。
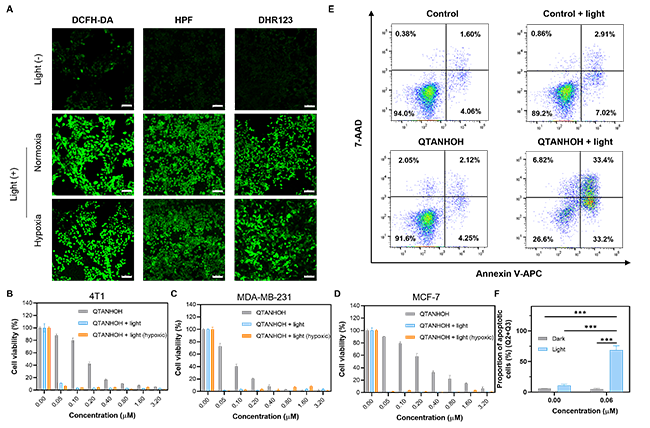
图3 胞内ROS检测和细胞毒性实验
进一步,研究队伍在原位乳腺癌小鼠模型上验证了QTANHOH的光动力治疗效果。实验组研究表明,经过一次光动力治疗能够有效地消融肿瘤,并能够激活肿瘤免疫微环境。给药不光照组也有中等程度的抑瘤率,这说明分子靶向光敏剂在体内也有良好的抑制HDAC活性的能力。此外,该分子能够有效抑制肿瘤的肺转移,也具有良好的生物安全性。
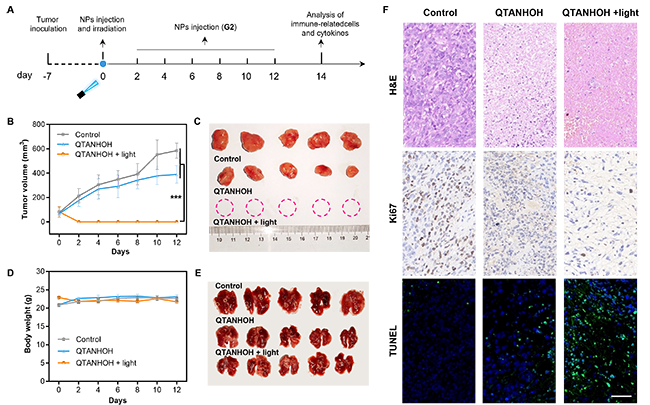
图4 小鼠原位乳腺癌的光动力治疗
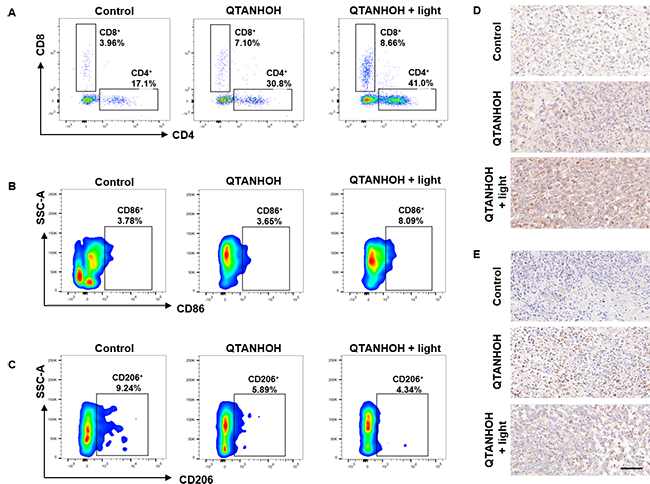
图5 抗肿瘤免疫分析
综上,施雷雷课题组报道了一种靶向HDAC的生物活性光敏剂,能够用于乏氧恶性肿瘤的光动力免疫治疗。该光敏剂QTANHOH可抑制HDAC活性,诱导细胞周期阻滞和凋亡。其光动力治疗效果在小鼠乳腺癌模型中得到验证,能够发挥很好的抑瘤作用且无明显毒性。此外,QTANHOH可以激活肿瘤的免疫微环境,增强光免疫治疗的效果。更重要的是,分子靶向光敏剂的设计策略为开发恶性肿瘤的多功能光疗药物提供了重要参考。
该成果于2023年12月11日发表于Advanced Functional Materials,论文通讯作者为上海交通大学医学院附属第一人民医院施雷雷研究员,团队博士后樊连峰为论文第一作者,上海市第一人民医院临床研究院疑难疾病精准研究中心为第一通讯作者单位。该研究得到了国家自然科学基金、上海市浦江人才计划、广东省自然科学基金、深圳市自然科学基金等项目资助。
论文题目:A Bioactive Photosensitizer for Hypoxia-Tolerant Molecular Targeting-Photo-Immunotherapy of Malignant Tumor
Lianfeng Fan, Chuanjiang Jian, Ling Li, Li Wang, Xuejiao Song, Minjia Wang, Chutong Liu, Xiaoxiao Liu, Shidang Xu, Xihui Gao*, Xianjie Shi, Miaomiao Yuan*, Bin Liu*, Leilei Shi*
Adv. Funct. Mater. 2023, DOI: 10.1002/adfm.202313755.
|
上一条:林达团队开发新型染色体外DNA(ecDNA)检测方法
下一条:李胜利团队与合作者解析视网膜母细胞瘤局部侵袭的单细胞转录组特征 |
返回列表 |